MÁQUINAS TÉRMICAS
lunes, 18 de julio de 2011
INTRODUCCIÓN
La segunda ley de la termodinámica, que se puede enunciar de diferentes formas equivalentes, tiene muchas aplicaciones prácticas. Desde el punto de vista de la ingeniería, tal vez la más importante es en relación con la eficiencia limitada de las máquinas térmicas. Expresada en forma simple, la segunda ley afirma que no es posible construir una máquina capaz de convertir por completo, de manera continua, la energía térmica en otras formas de energía.
Para comprender este planteamiento, es conveniente comenzar comentando acerca de las máquinas de movimiento perpetuo.
Para comprender este planteamiento, es conveniente comenzar comentando acerca de las máquinas de movimiento perpetuo.
MÁQUINAS DE MOVIMIENTO PERPETUO
Estas son máquinas hipotéticas que se clasifican en dos:
De primera especie: Son aquellas que violan la primera ley de la termodinámica, es decir, no conservan la energía, ya que hipotéticamente funcionan continuamente sin consumo de alguna forma de energía.
De segunda especie: Estas son máquinas que violan la segunda ley de la termodinámica, es decir, desarrollan Trabajo en forma cíclica (indefinida) intercambiando calor con una sola fuente térmica.
Para comprender este concepto es preciso conocer lo que son las:
MAQUINAS TERMICAS: Son aquellas que solo experimentan transferencia de energía en forma de calor y de trabajo con el medio. Estas se clasifican como:
• Bombas de calor
• Refrigeradores
Figura 1: IMAGEN DE UNA BOMBA DE CALOR
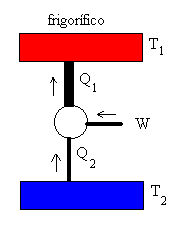
Figura 2: IMAGEN DE UN REFRIGERADOR
LAS BOMBAS DE CALOR: Son aquellas que transfieren calor desde una fuente térmica cálida a otra fría y realizan un trabajo hacia los alrededores.
Entendiéndose por fuente térmica, un sistema que tiene la misa temperatura en todos sus puntos y esta T no se afecta por transferencia de calor.
UN REFRIGERADOR, trabaja en sentido contrario a la Bomba de Calor, esto es, se refiere a que transfiere calos desde una fuente térmica fría a otra cálida, esto sólo puede ocurrir si los alrededores ejercen trabajo hacia el sistema.
PROTOTIPO DE MÁQUINAS TÉRMICAS CÍCLICAS ¨CICLO DE CARNOT¨
Fue inventado por el francés SADI CARNOT, consta de 4 etapas reversibles:
1. EXPANSIÓN ISOTERMICA
2. ESPANSIÓN ADIABÁTICA
3. COMPRESIÓN ISOTÉRMICA
4. COMPRESIÓN ADIABÁTICA
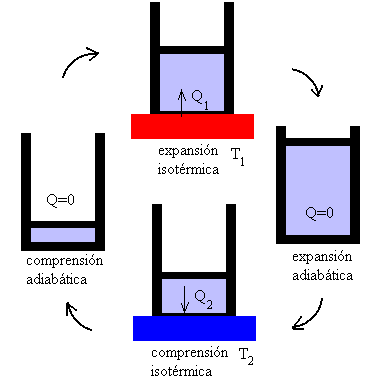
ESQUEMA DEL CICLO DE CARNOT
Figura 3: IMAGEN DEL ESQUEMA DE UN CICLO DE CARNOT
La representación gráfica del ciclo de Carnot en un diagrama PV se muestra en la figura 4, donde:
1. El proceso A-B es una expansión isotérmica a la temperatura TC, donde el gas se pone en contacto térmico con una fuente de calor a esa TC. Durante el proceso, el gas absorbe calor Qc de la fuente desde la base del cilindro y realiza trabajo Wab al subir el émbolo.
2. En el proceso B-C, la base del cilindro se reemplaza por una pared térmicamente no conductora y el gas se expande adiabáticamente. Durante el proceso la temperatura baja de TC a TF y el gas realiza trabajo Wbc al elevar el émbolo.
3. En el proceso C-D el gas se coloca en contacto térmico con una fuente de calor a temperatura TF y se comprime isotérmicamente a una temperatura
TF. Durante el proceso, el gas libera calor QF a la fuente y el trabajo realizado sobre el gas por un agente externo es Wcd.
4. En el proceso final D-A, la base del cilindro se reemplaza por una pared térmicamente no conductora y el gas se comprime adiabáticamente. La temperatura del gas aumenta de TF a TC y el trabajo realizado sobre el gas por un agente externo es Wda.
GRÁFICA DE PRESIÓN VS VOLUMEN
Figura 4: IMAGEN DE LA REPRESENTACIÓN ESQUEMÁTICA DEL CICLO DE CARNOT EN UN DIAGRAMA PV
Segunda ley de la termodinámica “postulado de Kelvin-Plank y postulado de clausius”
Postulado de Kelvin-Plank
Existen diferentes formas de enunciar la segunda ley de la termodinámica, pero en su versión más simple, establece que “el calor jamás fluye espontáneamente de un objeto frío a un objeto caliente”.
En la práctica, se encuentra que todas las máquinas térmicas sólo convierten una pequeña fracción del calor absorbido en trabajo mecánico. Por ejemplo un buen motor de un automóvil tiene una eficiencia aproximada de 20% y los motores diesel tienen una eficiencia en el rango de 35% a 40%. En base a este hecho, el enunciado de Kelvin – Planck de la segunda ley de la termodinámica es el siguiente:
“es imposible construir una máquina térmica que, operando en un ciclo, no tenga otro efecto que absorber la energía térmica de una fuente y realizar la misma cantidad de trabajo”.
Figura 5: MÁQUINA TÉRMICA DE Kelvin – Planck
Esto es equivalente a afirmar que “es imposible construir una máquina de movimiento perpetuo (móvil perpetuo) de segunda clase”, es decir, una máquina que pudiera violar la segunda ley de la termodinámica. (Una máquina de movimiento perpetuo de primera clase es aquella que puede violar la primera ley de la termodinámica (conservación de la energía), también es imposible construir una máquina de este tipo). La figura 5 es un diagrama esquemático de una máquina térmica perfecta imposible de construir.
Un refrigerador es una máquina térmica que opera en sentido inverso, como se muestra de manera esquemática en la figura 2. La máquina absorbe calor QF de la fuente fría y entrega calor QC a la fuente cálida. Esto sólo puede ser posible si se hace trabajo sobre el refrigerador. De la primera ley, se ve que el calor cedido a la fuente caliente debe ser igual a la suma del trabajo realizado y el calor absorbido de la fuente fría. Por lo tanto, se ve que el refrigerador transfiere calor del cuerpo más frío a un cuerpo más cálido (la cocina).
Enunciado de Clausius de la segunda ley de la termodinámica.
Resulta deseable construir un refrigerador que pueda realizar su proceso con el mínimo de trabajo. Si se pudiera construir uno donde el proceso de refrigeración se realice sin ningún trabajo, se tendría un refrigerador perfecto. Esto es imposible, porque se violaría la segunda ley de la termodinámica, que es el enunciado de Clausius de la segunda ley (Rudolf Clausius, alemán, 1822 -1888):
“es imposible construir una máquina cíclica, que no tenga otro efecto que transferir calor continuamente de un cuerpo hacia otro, que se encuentre a una temperatura más elevada”.
En términos sencillos, el calor no puede fluir espontáneamente de un objeto frío a otro cálido. Este enunciado de la segunda ley establece la dirección del flujo de calor entre dos objetos a diferentes temperaturas. El calor sólo fluirá del cuerpo más frío al más cálido si se hace trabajo sobre el sistema.
Aparentemente los enunciados de Kelvin – Planck y de Clausius de la segunda ley no están relacionados, pero son equivalentes en todos sus aspectos. Se puede demostrar (pero aquí no lo hacemos) que si un enunciado es falso, el otro también lo es.
De primera especie: Son aquellas que violan la primera ley de la termodinámica, es decir, no conservan la energía, ya que hipotéticamente funcionan continuamente sin consumo de alguna forma de energía.
De segunda especie: Estas son máquinas que violan la segunda ley de la termodinámica, es decir, desarrollan Trabajo en forma cíclica (indefinida) intercambiando calor con una sola fuente térmica.
Para comprender este concepto es preciso conocer lo que son las:
MAQUINAS TERMICAS: Son aquellas que solo experimentan transferencia de energía en forma de calor y de trabajo con el medio. Estas se clasifican como:
• Bombas de calor
• Refrigeradores
Figura 1: IMAGEN DE UNA BOMBA DE CALOR
Figura 2: IMAGEN DE UN REFRIGERADOR
LAS BOMBAS DE CALOR: Son aquellas que transfieren calor desde una fuente térmica cálida a otra fría y realizan un trabajo hacia los alrededores.
Entendiéndose por fuente térmica, un sistema que tiene la misa temperatura en todos sus puntos y esta T no se afecta por transferencia de calor.
UN REFRIGERADOR, trabaja en sentido contrario a la Bomba de Calor, esto es, se refiere a que transfiere calos desde una fuente térmica fría a otra cálida, esto sólo puede ocurrir si los alrededores ejercen trabajo hacia el sistema.
PROTOTIPO DE MÁQUINAS TÉRMICAS CÍCLICAS ¨CICLO DE CARNOT¨
Fue inventado por el francés SADI CARNOT, consta de 4 etapas reversibles:
1. EXPANSIÓN ISOTERMICA
2. ESPANSIÓN ADIABÁTICA
3. COMPRESIÓN ISOTÉRMICA
4. COMPRESIÓN ADIABÁTICA
ESQUEMA DEL CICLO DE CARNOT
Figura 3: IMAGEN DEL ESQUEMA DE UN CICLO DE CARNOT
La representación gráfica del ciclo de Carnot en un diagrama PV se muestra en la figura 4, donde:
1. El proceso A-B es una expansión isotérmica a la temperatura TC, donde el gas se pone en contacto térmico con una fuente de calor a esa TC. Durante el proceso, el gas absorbe calor Qc de la fuente desde la base del cilindro y realiza trabajo Wab al subir el émbolo.
2. En el proceso B-C, la base del cilindro se reemplaza por una pared térmicamente no conductora y el gas se expande adiabáticamente. Durante el proceso la temperatura baja de TC a TF y el gas realiza trabajo Wbc al elevar el émbolo.
3. En el proceso C-D el gas se coloca en contacto térmico con una fuente de calor a temperatura TF y se comprime isotérmicamente a una temperatura
TF. Durante el proceso, el gas libera calor QF a la fuente y el trabajo realizado sobre el gas por un agente externo es Wcd.
4. En el proceso final D-A, la base del cilindro se reemplaza por una pared térmicamente no conductora y el gas se comprime adiabáticamente. La temperatura del gas aumenta de TF a TC y el trabajo realizado sobre el gas por un agente externo es Wda.
GRÁFICA DE PRESIÓN VS VOLUMEN
Figura 4: IMAGEN DE LA REPRESENTACIÓN ESQUEMÁTICA DEL CICLO DE CARNOT EN UN DIAGRAMA PV
Segunda ley de la termodinámica “postulado de Kelvin-Plank y postulado de clausius”
Postulado de Kelvin-Plank
Existen diferentes formas de enunciar la segunda ley de la termodinámica, pero en su versión más simple, establece que “el calor jamás fluye espontáneamente de un objeto frío a un objeto caliente”.
En la práctica, se encuentra que todas las máquinas térmicas sólo convierten una pequeña fracción del calor absorbido en trabajo mecánico. Por ejemplo un buen motor de un automóvil tiene una eficiencia aproximada de 20% y los motores diesel tienen una eficiencia en el rango de 35% a 40%. En base a este hecho, el enunciado de Kelvin – Planck de la segunda ley de la termodinámica es el siguiente:
“es imposible construir una máquina térmica que, operando en un ciclo, no tenga otro efecto que absorber la energía térmica de una fuente y realizar la misma cantidad de trabajo”.
Figura 5: MÁQUINA TÉRMICA DE Kelvin – Planck
Esto es equivalente a afirmar que “es imposible construir una máquina de movimiento perpetuo (móvil perpetuo) de segunda clase”, es decir, una máquina que pudiera violar la segunda ley de la termodinámica. (Una máquina de movimiento perpetuo de primera clase es aquella que puede violar la primera ley de la termodinámica (conservación de la energía), también es imposible construir una máquina de este tipo). La figura 5 es un diagrama esquemático de una máquina térmica perfecta imposible de construir.
Un refrigerador es una máquina térmica que opera en sentido inverso, como se muestra de manera esquemática en la figura 2. La máquina absorbe calor QF de la fuente fría y entrega calor QC a la fuente cálida. Esto sólo puede ser posible si se hace trabajo sobre el refrigerador. De la primera ley, se ve que el calor cedido a la fuente caliente debe ser igual a la suma del trabajo realizado y el calor absorbido de la fuente fría. Por lo tanto, se ve que el refrigerador transfiere calor del cuerpo más frío a un cuerpo más cálido (la cocina).
Enunciado de Clausius de la segunda ley de la termodinámica.
Resulta deseable construir un refrigerador que pueda realizar su proceso con el mínimo de trabajo. Si se pudiera construir uno donde el proceso de refrigeración se realice sin ningún trabajo, se tendría un refrigerador perfecto. Esto es imposible, porque se violaría la segunda ley de la termodinámica, que es el enunciado de Clausius de la segunda ley (Rudolf Clausius, alemán, 1822 -1888):
“es imposible construir una máquina cíclica, que no tenga otro efecto que transferir calor continuamente de un cuerpo hacia otro, que se encuentre a una temperatura más elevada”.
En términos sencillos, el calor no puede fluir espontáneamente de un objeto frío a otro cálido. Este enunciado de la segunda ley establece la dirección del flujo de calor entre dos objetos a diferentes temperaturas. El calor sólo fluirá del cuerpo más frío al más cálido si se hace trabajo sobre el sistema.
Aparentemente los enunciados de Kelvin – Planck y de Clausius de la segunda ley no están relacionados, pero son equivalentes en todos sus aspectos. Se puede demostrar (pero aquí no lo hacemos) que si un enunciado es falso, el otro también lo es.
Suscribirse a:
Comentarios (Atom)